2.11. Šķīdumu pH. Neitralizācijas reakcijas
pH ir lielums, kas raksturo ūdeņraža jonu (H+)
koncentrāciju šķīdumā.
pH vērtība ir nozīmīga dažādu bioķīmisku reakciju norisē dzīvajos organismos, kā arī ķīmisku procesu norisē dabā un tehnikā.
Jēdzienu pH ieviesa dāņu ķīmiķis Sērensens 1909.gadā. Tā burti ir ņemti no latīņu valodas vārdiem „pondus hydrogenii”, kas nozīmē „ūdeņraža svars”. pH rāda ūdeņraža jonu koncentrāciju šķīdumā.
pH vērtības ir no 1 līdz 14. Ja pH vērtība ir mazāka par 7 ūdens šķīdums ir skābs, ja pH vērtība ir lielāka par 7, ūdens šķīdums ir bāzisks. Neitrāla šķīduma pH vērtība ir 7.
Tabulā ir doti dažu vielu šķīdumu pH:
| Viela
|
Kuņģa sula
|
Etiķis
|
Kafija
|
Piens
|
Destilēts ūdens
|
Asinis
|
Jūras ūdens
|
Ziepes
|
Ožamais spirts
|
Veļas soda
|
| pH
|
1,5
|
2,9
|
5,0
|
6,8
|
7,0
|
7,4
|
8,0
|
9,0
|
11,5
|
13,5
|
Šķīduma pH var noteikt divējādi:
- izmantojot atsevišķus indikatorus
tādus kā - lakmuss, fenolftaleīns, metiloranžs, universālindikators, kuri maina krāsu atkarībā no vides pH.
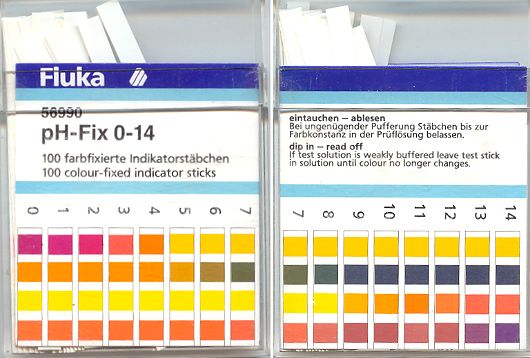
Parnesama indikatoru skala ir izmantojama dažādās vidēs
 Universālindikatoru skala
http://genchem.chem.wisc.edu/demonstrations
Universālindikatoru skala
http://genchem.chem.wisc.edu/demonstrations
- lietojot pH-metru.
Tas ir elektrisks aparāts, ar kuru var precīzi izmērīt šķīduma pH.
 PH-Mēraparāts TESTO205 SET
PH-Mēraparāts TESTO205 SET
http://www.conrad.de/script/ph_messgerat_testo205.sap
Reakcijas starp skābēm un bāzēm sauc par neitralizācijas reakcijām. Skābam šķīdumam reaģējot ar bāzisku šķīdumu, rodas neitrāls šķīdums. Neitralizācijas procesa galaprodukts ir ūdens.
Neitralizācijas procesu attēlo jonu reakcijas vienādojums: H
+ + OH
-
→ H
2O
Neitralizācijas procesus var vērot arī dabā – organismos, atmosfērā, augsnē.
Piemērs. Augu augšanai svarīgs ir augsnes pH. Augiem ir traucēta normāla attīstība, ja augsnes pH vērtība ir mazāka par 6,0 vai lielāka par 8,0. Augsnes skābumu var neitralizēt, iestrādājot tajā bāziskas vielas. Parasti lieto kalcija oksīdu CaO (nedzēstos kaļķus) vai kalcija hidroksīdu Ca(OH)
2 (dzēstos kaļķus). Daudzu ezeru ūdeņi paskābinās, jo tajos nonāk gaisā esošās skābes. Palielināts skābes daudzums ūdenī var ietekmēt tajā mītošos dzīvos organismus. Zivis var iet bojā. Ezeru ūdeni iespējams neitralizēt, nogremdējot tajos kaļķakmeņa gabalus.